第2节 热力学第一定律知识点归纳 知识点一、热力学第一定律 1.热力学第一定律 (1)内容:一个热力学系统的内能增量等于外界向它传递的热量与外界对它所做的功的和. (2)公式:ΔU=Q+W. 2.对公式ΔU=Q+W中各物理量符号的规定
3.热力学第一定律应用中几种特殊情况的探讨 (1)绝热做功过程中,Q=0,ΔU=W,外界对物体做的功等于物体内能的增加量. (2)若过程中不做功只传热,W=0,则ΔU=Q,物体吸收的热量等于物体内能的增加量. (3)若过程的始末状态物体的内能不变,ΔU=0,即W+Q=0,则W=-Q,外界对物体做的功等于物体放出的热量;或Q=-W,物体吸收的热量等于物体对外界做的功. 知识点二、对理想气体应用热力学第一定律 (1)对于理想气体来说,因不考虑分子势能,故其内能为所有分子动能的总和(即等于分子数与分子热运动的平均动能的乘积).内能仅由分子数与温度决定,因此对于一定质量的理想气体来说,内能是否变化取决于其温度是否变化,升温,ΔU为正,降温,ΔU为负,温度不变,ΔU=0. (2)理想气体是否做功,取决于其体积的变化.若体积变大,则为气体对外界做功;体积变小,则为外界对气体做功;体积不变,则做功为零. (3)热量Q取决于容器是绝热的还是导热的,并不是温度升高吸热,温度降低放热. (4)外界对理想气体做功或理想气体对外界做功时,若恒压膨胀,即压强不变时,功的计算公式为W=pΔV.(p为理想气体的压强、ΔV为理想气体体积的变化量.) 典例分析 一、做功和热传递
A.Q1-Q2=W2-W1 B.Q1=Q2 C.W1=W2 D.Q1>Q2 解析 本题所考查的内容涉及理想气体的内能、改变物体内能的两种方式及热力学第一定律等知识.解答本题的切入点是,对一定质量的理想气体,在某一状态下其内能是确定的.首先,对一定质量的理想气体,经过一系列的状态变化后又回到原状态,表明整个过程中内能的变化为零,即通过做功和热传递引起的内能变化相互抵消,所以A选项正确.当然,若Q1=Q2,则必定有W1=W2;若Q1>Q2,则必定有W1<W2;若Q1<Q2,则必定有W1>W2,所以B、C、D三项都有可能,故选A. 答案 A 二、热力学第一定律的应用
(1)物体的内能是增加还是减少?变化量是多少? (2)分子势能是增加还是减少? (3)分子的平均动能是增加还是减少? 解析 (1)气体从外界吸热为Q=4.2×105J 气体对外做功W=-6×105J 由热力学第一定律 ΔU=W+Q=(-6×105J)+(4.2×105J)=-1.8×105J ΔU为负,说明气体的内能减少了。 所以,气体内能减少了1.8×105J。 (2)因为气体对外做功,所以气体的体积膨胀,分子间的距离增大了,分子力做负功,气体分子势能增加了。 (3)因为气体内能减少,同时气体分子势能增加,说明气体分子的平均动能一定减少了。 答案 (1)减少 1.8×105J (2)增加 (3)减少
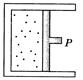
A.W=8×104 J,ΔU=1.2×105 J,Q=4×104 J B.W=8×104 J,ΔU=-1.2×105 J,Q=-2×105 J C.W=-8×104 J,ΔU=1.2×105 J,Q=2×104 J D.W=-8×104 J,ΔU=-1.2×105 J,Q=-4×104 J 解析 因为外界对气体做功,W取正值,即W=8×104 J;内能减少,ΔU取负值,即ΔU=-1.2×105 J;根据热力学第一定律ΔU=W+Q,可知Q=ΔU-W=-1.2×105 J-8×104 J=-2×105 J,B选项正确. 答案 B 自我检测 1.在一个与外界没有热交换的房间内打开冰箱门,冰箱正常工作,过一段时间房间内的温度将( ) A.降低 B.升高 C.不变 D.无法确定 解析 取房间内气体及电冰箱(有散热装置)为系统,外界消耗电能,对系统做功,系统总内能增加。 答案 B 2.气体膨胀对外做功100J,同时从外界吸收了120J的热量,它的内能的变化可能是( ) A.减小20J B.增大20J C.减小220J D.增大220J 解析 研究对象为气体。依符号规则,对外做功W=-100J,吸收热量Q=120J。由热力学第一定律有ΔU=W+Q=-100J+120J=20J。ΔU>0,说明气体的内能增加。 答案 B 3.如图是密闭的气缸.外力推动活塞P压缩气体,对缸内气体做功800 J,同时气体向外界放热200 J,缸内气体的( )
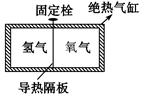
A.温度升高,内能增加600 J B.温度升高,内能减少200 J C.温度降低,内能增加600 J D.温度降低,内能减少200 J 解析 由题意知W=800 J,Q=-200 J,由热力学第一定律,得ΔU=W+Q=600 J,可见内能增加600 J.因气体的内能仅是温度的函数,内能增加,则温度升高,故A项正确. 答案 4.对于一定质量的物体(或系统),有( ) A.吸热物体的温度一定会升高 B.只要气体的体积、温度变化,则气体的内能一定改变 C.外界对系统做功,系统内能可能不变 D.物体温度不变,则其内能一定也不变 解析 物体的内能是否改变在于系统吸热和做功的总和,所以A、D两项错误;物体的体积和温度改变,不能确定其内能是否改变,故B项错误,C项正确. 答案 C 5.如下图所示,绝热气缸中间用固定栓将可无摩擦移动的导热隔板(质量不计)固定,左右两室分别充有一定量的氢气和氧气(视为理想气体).初始时,两室气体的温度相等,氢气的压强大于氧气的压强,松开固定栓直至系统重新达到平衡.下列说法中正确的是( )
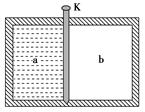
A.初始时氢气分子的平均动能大于氧分子的平均动能 B.系统重新达到平衡时,氢气的内能比初始时的小 C.松开固定栓直至系统重新达到平衡的过程中,有热量从氧气传递到氢气 D.松开固定栓直至系统重新达到平衡的过程中,氧气的内能先增大后减小 解析 初始时,两室气体的温度相同,故分子平均动能相等,A错;因为气缸是绝热的,所以气缸内气体的总的内能守恒,由于隔板导热,重新平衡后两种气体温度仍相同,即气体内能仍相等,所以每种气体内能均不变,B错;氢气通过隔热板对氧气做功,而内能不变,由热力学第一定律可知氢气一定吸收了来自氧气的热量,C正确;达到平衡的过程中,氢气对氧气做功,氧气内能增加;热量从氧气传递到氢气,氧气内能又减小,D正确. 答案 CD 6.如图所示,一绝热容器被隔板K隔开成a、b两部分.已知a内有一定量的稀薄气体,b内为真空.抽开隔板K后,a内气体进入b,最终达到平衡状态.在此过程中( )
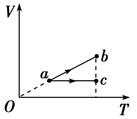
A.气体对外界做功,内能减少 B.气体不做功,内能不变 C.气体压强变小,温度降低 D.气体压强变小,温度不变 解析 因b内为真空,抽开隔板K后,a内气体对外界不做功,由ΔU=W+Q知内能不变,故选项A错误、选项B正确.稀薄气体可看作理想气体,其内能只与温度有关,气体的内能不变,温度也不变,由p1V1=p2V2和V1<V2知p1>p2,即气体压强变小,故选项C错误、选项D正确. 答案 BD 7.带有活塞的汽缸内封闭一定量的理想气体.气体开始处于状态a;然后经过过程ab到达状态b,或经过过程ac到达状态c,b、c状态温度相同,如V—T图所示.设气体在状态b和状态c的压强分别为pb和pc,在过程ab和ac中吸收的热量分别为Qab和Qac,则( )
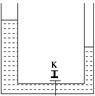
A.pb>pc,Qab>Qac B.pb>pc,Qab<Qac C.pb<pc,Qab>Qac D.pb<pc,Qab<Qac 解析 V—T图线的斜率越大,压强p越小,故pb<pc.由热力学第一定律有:Q=ΔU-W,因Tb=Tc,所以ΔUab=ΔUac,而Wab>Wac,故Qab>Qac.综上可知C项正确. 答案 C 8.一定量的理想气体在某一过程中,从外界吸收热量2.5×104 J,气体对外界做功1.0×104 J,则该理想气体的( ) A.温度降低,密度增大 B.温度降低,密度减小 C.温度升高,密度增大 D.温度升高,密度减小 解析 由ΔU=W+Q可得理想气体内能变化:ΔU=-1.0×104 J+2.5×104 J=1.5×104 J>0,故温度升高,A、B两项均错.因为气体对外做功,所以气体一定膨胀,体积变大,由ρ=可知密度变小,故C项错误,D项正确. 答案 D 9.如图所示的两端开口的U形管中,盛有同种液体,并用阀门K将液体隔成左、右两部分,左边液面比右边液面高.现打开阀门K,从打开阀门到两边液面第一次平齐的过程中,液体向外放热为Q,内能变化量为ΔU,动能变化量为ΔEk;大气对液体做功为W1,重力做功为W2,液体克服阻力做功为W3,由功能关系可得:
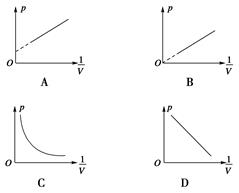
①W1=0 ②W2-W3=ΔEk ③W2-W3=Q=ΔU ④W3-Q=ΔU 其中正确的是( ) A.①②③ B.①②④ C.②③ D.①③ 解析 由动能定理可知W2-W3+W1=ΔEk,其中W1=p·ΔV左-p·ΔV右=0,可知①、②正确.由热力学第一定律ΔU=W+Q得ΔU=W3+Q,可知④正确、③错误.综合以上分析可知B正确. 答案 B 10.对于一个大气压下100 ℃的水变成100 ℃的水蒸气的过程中,下列说法正确的是( ) A.水的内能增加,对外界做功,一定是吸热 B.水的内能不变,对外界做功,从外界吸热 C.水的内能减少,对外界不做功,向外界放热 D.水的内能增加,对外界做功,向外界放热 解析 水变成蒸汽的过程是吸热的过程,又因气体膨胀对外界做功,分子间距增大,分子势能增加,分子动能不变,由此判断可知A对. 答案 A 11.(1)为了将空气装入气瓶内,现将一定质量的空气等温压缩,空气可视为理想气体。下列图象能正确表示该过程中空气的压强p和体积V关系的是________。
(2)在将空气压缩装入气瓶的过程中,温度保持不变,外界做了24 kJ的功。现潜水员背着该气瓶缓慢地潜入海底,若在此过程中,瓶内空气的质量保持不变,且放出了5 kJ的热量。在上述两个过程中,空气的内能共减小________kJ,空气________(选填“吸收”或“放出”)的总热量为________kJ。 解析 (1)根据玻意耳定律pV=C,故选项B正确。 (2)将空气压缩装入气瓶的过程中,温度不变,所以内能不变,潜水员背着气瓶潜入海底的过程中,放出5kJ的热量,则ΔU=-5kJ。故两过程减小的空气内能为5kJ,在这两个过程中,由热力学第一定律得ΔU=W+Q,Q=ΔU-W=(-5-24)kJ=-29kJ,“-”说明放出热量。 答案 (1)B (2)5 放出 29
|